
随着临床试验安全性法规的不断完善和药物警戒实践的深化,对严重不良事件(SAE)的高效管理需求日益迫切。临床研究团队常面临多项目SAE信息管理的挑战,包括数据的重复录入、紧急上报和SAE一致性核查耗时耗力等问题。
SAE在线填报系统提供了一站式解决方案,使各研究中心能够在线填报SAE报告、在线审批、电子签名、在线质疑,并支持同步发送数据至PV(药物警戒)系统和EDC(临床试验电子数据采集)系统,实现了数据的无缝同步,解决了数据重复录入的问题。此外,可以定期推送SAE一致性核查报表,大幅度减少了DM、PV团队的核查工时。
SAE全流程管理
产品优势
即刻签署,高效上报
研究者可通过手机扫描二维码轻松完成SAE报告的电子签名,签名后的报告即刻以PDF格式自动发送至PV系统,并第一时间以邮件形式通知申办方,减少了沟通成本。
系统互通、智能同步
eSAE系统与EDC和PV系统互联,SAE数据一旦在eSAE中填报,即刻同步至PV系统,并自动回填至EDC系统,彻底消除了重复录入的繁琐,确保数据的一致性和准确性。
质疑交互,及时反馈
开放PV人员在eSAE系统中提交质疑的权限,PV团队可在线发送SAE质疑信至相应中心的研究者/CRC,实现SAE报告质疑的线上处理,加快问题解决的速度。
全量管理、合规无忧
SAE报告的中心在线填报,实现从数据录入到核查的全流程管理,并通过自动化一致性比对,确保数据的准确性。同时数据留痕,并支持数据导出,确保了数据的可追溯性和透明度,全面满足法规要求。
个性定制、灵活高效
可根据特定的研究需求和标准,定制SAE原始报告表模板,SAE一致性核查报表等,并持续优化创新,让SAE管理更加高效、便捷。
核心功能
1
SAE报告信息录入、审核、评估
2
SAE报告电子签批,生成签名的PDF附件
3
SAE报告自动同步PV系统
4
SAE数据自动回填EDC系统
5
PV人员与中心人员在线处理SAE相关质疑
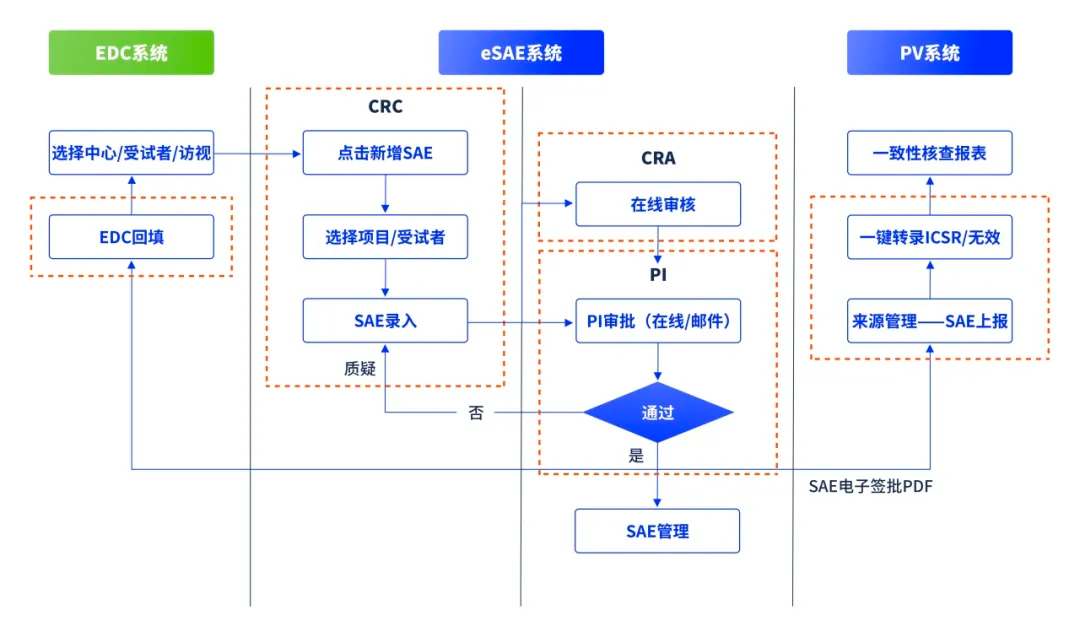
用户可通过百奥知EDC进入eSAE系统,受试者信息可直接同步到SAE录入页面,无需重新录入,或通过独立的eSAE入口单独使用。
Bioknow eSAE标志着临床试验SAE管理的新纪元,我们期待与您携手开启这一数字化革新之旅。百奥知药物警戒团队诚邀行业同仁共同推进PV信息化进程,共创高效、合规的临床试验环境。